El descubrimiento del electrón por J.J. Thomson
Los experimentos sobre descargas eléctricas a través de gases permitieron conocer la estructura del átomo.
A finales del siglo XIX, el científico J.J. Thomson comenzó a hacer experimentos con algo llamado tubos de rayos catódicos. Estos son básicamente tubos de vidrio sellados en los que se ha quitado la mayor parte del aire.
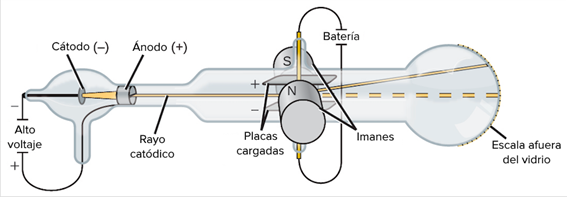
Cuando aplicas un voltaje alto entre dos electrodos, uno en cada lado del tubo, empieza a fluir un rayo de partículas desde el cátodo (que es el electrodo con carga negativa) hacia el ánodo (el electrodo con carga positiva). Son los llamados "tubos de rayos catódicos" porque el rayo de partículas o "rayo catódico" comienza en el cátodo. Puedes ver este rayo si pintas el extremo del tubo correspondiente al ánodo con algún material fosforescente. Cuando el rayo catódico golpea el material fosforescente, este produce una chispa o emite luz.
|

|
Para entender más sobre estas partículas que había descubierto, Thomson hizo experimentos muy interesantes. Puso el tubo de rayos catódicos entre dos placas con cargas opuestas y notó que el rayo se movía, alejándose de la placa cargada negativamente y acercándose a la placa cargada positivamente. De esto, Thomson pensó que el rayo estaba hecho de partículas con carga negativa.
También usó imanes y vio que el campo magnético desviaba el rayo catódico. Con estos experimentos, Thomson pudo calcular la relación entre la carga y la masa de estas partículas. Lo increíble fue que descubrió que la masa de cada partícula era mucho menor que la de cualquier átomo conocido.
Thomson probó con diferentes metales para los electrodos y descubrió que las propiedades del rayo catódico permanecían iguales, sin importar el material del que provinieran.
De sus experimentos, Thomson llegó a algunas conclusiones importantes:
- El rayo catódico está hecho de partículas con carga negativa.
- Estas partículas deben ser parte de los átomos, porque la masa de cada partícula es solo una pequeña fracción de la masa de un átomo de hidrógeno.
- Estas partículas subatómicas están presentes en todos los átomos de los diferentes elementos.
Aunque controvertida en ese momento, la idea de Thomson fue gradualmente aceptada, y su partícula de rayos catódicos es lo que ahora llamamos un electrón, una partícula subatómica cargada negativamente con una masa más de mil veces menor que la de un átomo.
Este descubrimiento contradecía parte de la teoría atómica de Dalton, que decía que los átomos eran indivisibles. Para explicar esto, se necesitaba un nuevo modelo atómico.
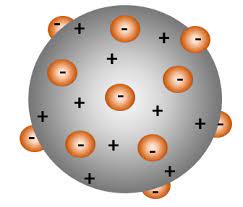
En el modelo atómico de Thomson, el átomo es una esfera de masa positiva uniforme, en la que se encuentran insertas las cargas negativas (los electrones), lo que explica la neutralidad eléctrica de la materia. Este modelo fue conocido como pudin de pasas.